by
¿Qué es la optogenética?
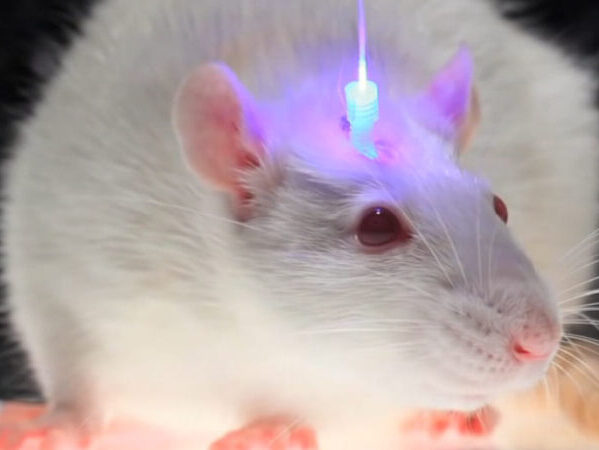
La optogenética combina métodos ópticos (destellos de luz provenientes de un láser o un LED) con métodos genéticos para transferir a un grupo específico de neuronas el cDNA que codifica proteínas de origen microbiano sensibles a la luz (llamadas opsinas). Ésta es una tecnología de vanguardia que inició su desarrollo en el 2005 por el Dr. Karl Deisserothde la Universidad de Stanford. En el 2010 la revista Nature Methods lo nombró el método más importante del año.
La aproximación optogenética se basa en la introducción en las células de genes exógenos que codifican proteínas fotosensibles, las cuales sirven para modificar el comportamiento celular mediante la luz. Por lo tanto, la tecnología optogenética abarca el desarrollo de: 1) esas proteínas sensibles a la luz (las herramientas básicas del sistema), 2) la puesta a punto de estrategias para introducir los genes en las células o tejidos diana y 3) la generación de sistemas de lectura capaces de analizar los cambios de comportamiento que se produzcan en la célula del tejido o animal del que se trate.
Aplicaciones de la optogenética
Este método servirá para identificar a las poblaciones celulares implicadas en diversos padecimientos y apoyará la búsqueda de nuevos tratamientos.
- Ha servido para controlar ataques epilépticos en modelos animales experimentales.
- Al manipular las neuronas dopaminérgicas se ha podido potenciar o evitar la adicción a la cocaína.
- El sueño y el estado de vigilia pueden regularse a través de las neuronas hipocretinas . Es la base para el desarrollo de fármacos que ayuden al tratamiento de la narcolepsia.

- También se puede inducir el apetito al activar neuronas del hipotálamo o inhibirlo y producir pérdida de peso.
- Si se produce una arritmia cardíaca, el corazón nuevamente puede bombear sangre al ritmo de la luz. De hecho, se ha desarrollado el primer marcapasos basado en la optogenética.
- Tratamiento del Parkinson
- Estos métodos han permitido recuperar la vista a ratones ciegos.
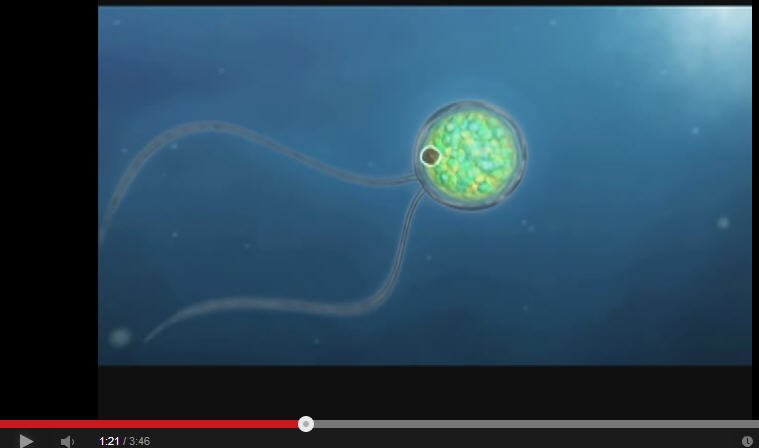
Las bases de la optogenética se encuentran en el estudio de un organismo unicelular, el alga Chlamydomonas reinhardtii y su capacidad para moverse hacia una fuente luminosa. Los doctores Peter Hegemann, Georg Nagel, y Ernst Bamberg descubrieron una proteína llamada Channelrodopsina 2 (ChR2) de la cual esta alga se vale, para desplazarse hacia la luz.
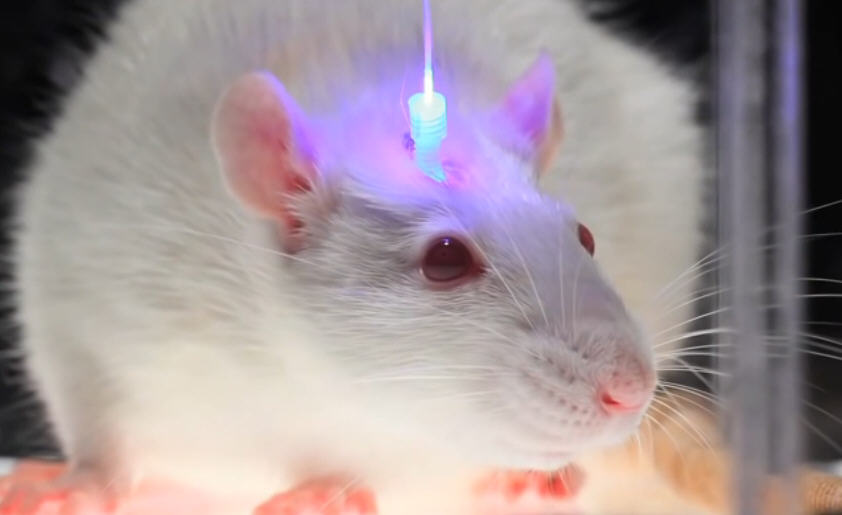
Ante la estimulación con un haz luminoso de 473nm (luz azul), el ChR2 se abre permitiendo el paso de iones a través del gradiente electroquímico de la célula (H+>Na+>K+>Ca+). Las neuronas expresan niveles suficientes de ChR2 para que la luz azul, vía fibra óptica, permita la apertura del canal y la entrada de sodio al interior de la neurona. Cuando el ChR2 se expresa en la membrana neuronal se transforman los impulsos luminosos en potenciales de acción.
Cómo funciona
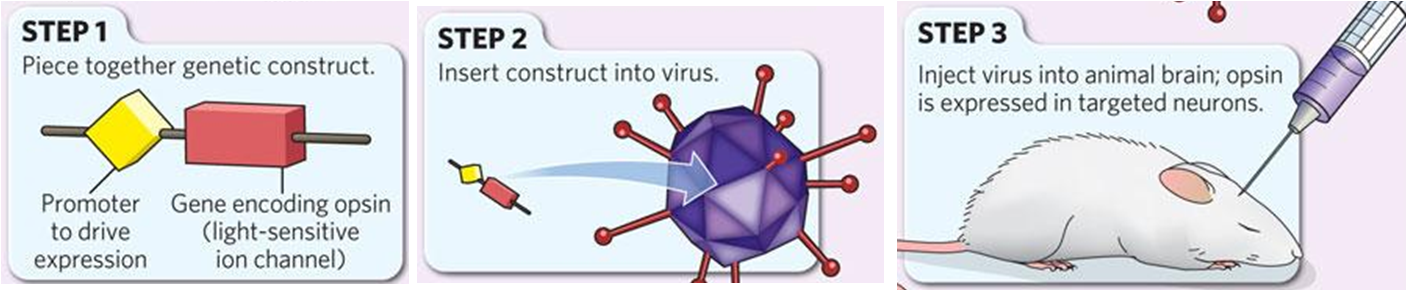
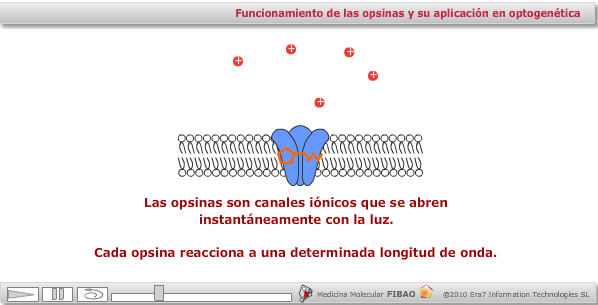
Todos conocemos moléculas que pueden activarse en respuesta a la luz, como la clorofila que se encuentra en las plantas, o las rodopsinas en los conos de la retina. Las que se emplean en los modelos optogenéticos suelen proceder de bacterias, y pueden ser de varios tipos, pero en general constituyen lo que se denomina canales iónicos. Es decir, que cuando se activa esa proteína se abre un poro en la membrana en la que se encuentra embebida y permite el paso específico de iones a través de la membrana de la célula en cuestión. Así, dependiendo del tipo de canal iónico que expresemos en una neurona podremos hacer que ésta se active (si el canal es de calcio o de sodio) o que se inhiba (si es de potasio).
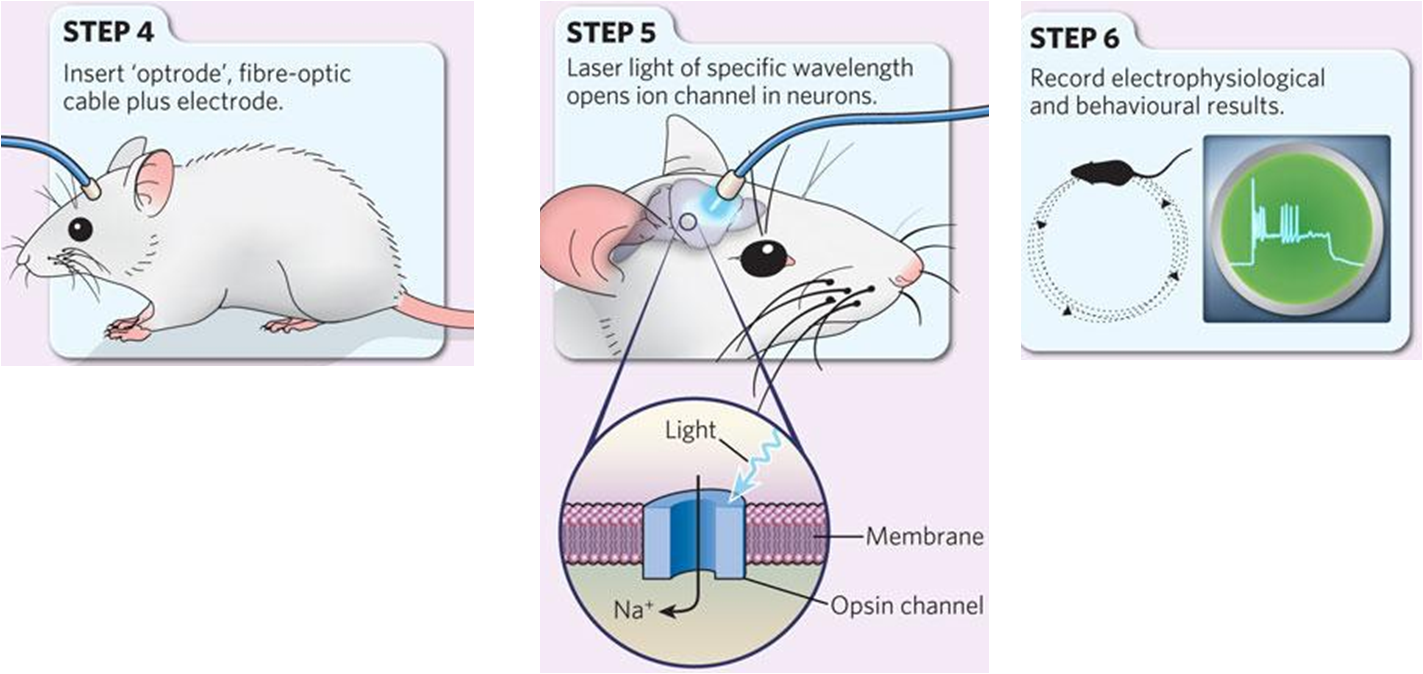
NATUREVol 29 April 2010
El siguiente paso consistirá en secuenciar el gen que contiene la información que se codifica en las bacterias para esos canales e insertarlo en las neuronas que nosotros queramos. Esto se consigue inyectando un virus en el cerebro de los animales. Dichos virus obtenidos mediante ingeniería genética transportan, no sólo la información genética necesaria para generar la proteína deseada, sino además una secuencia (denominada promotor) que permite que esa proteína se exprese solamente en las neuronas que nosotros queramos (si no, correríamos el riesgo de que la proteína se insertase en cualquier célula del organismo). Una vez que tenemos a nuestro animal expresando la proteína que queríamos y en los tipos neuronales deseados, el siguiente paso será activar esas proteínas. ¿Cómo hacerlo? Pues implantando al animal, un cable de fibra óptica mediante cirugía estereotáxica, para que llegue hasta la región del cerebro cuya actividad queremos modular. El siguiente paso consistiría en conectar esa fibra óptica a una fuente de luz. Y la mejor forma de conseguir una fuente de luz de una longitud de onda determinada es emplear un láser. A partir de ahí ya todo consiste en encender o apagar la luz y medir lo que se nos antoje, como una determinada conducta, ciertos marcadores bioquímicos que sospechemos que pueden variar cuando activamos esas células, o incluso respuestas eléctricas en otras regiones del cerebro que pensemos que pueden estar conectadas con las neuronas cuya actividad estamos modulando.
Fuentes : http://www.nature.com/news/2010/100505/full/465026a.htmlhttp://cerebrodarwin.blogspot.com.es/2011/04/method-of-year-2010-optogenetics-by_06.htmlhttp://ayp.calypso-media.com/infografia/optogenetica.htmlhttp://medmol.es/tecnicas/optogenetica/ Ana Abad TorrentAdjunta del Servicio de Anestesia del Hospital de Viladecans. Barcelona.__________El autor declara que el manuscrito no ha recibido financiación, no existe conflicto de intereses y no aparecen datos de pacientes.