Magnetismo
Alerta la agencia estadounidense por tormenta geomagnética severa para este 24 de marzo
Fuente: YouTube La agencia estadounidense ha observado un elevado CME correspondiente a una tormenta geomagnética severa sobre la Tierra y…
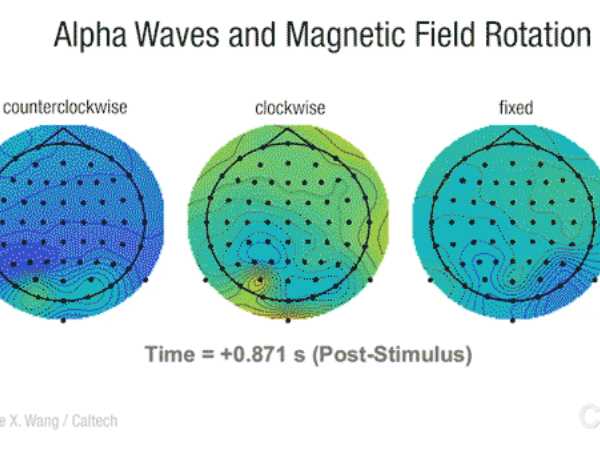
Nuestro cerebro reacciona a las variaciones del campo magnético terrestre
Fuente: Tendencias 21 El cerebro humano es capaz de reaccionar a las variaciones en el campo magnético terrestre, por lo…
Los campos magnéticos afectan a la excitabilidad del cerebro
Fuente: Neurología.com El contacto de un imán potente aplicado durante 10 minutos directamente sobre el cuero cabelludo puede provocar una…
Energía magnética
Fuente: Concepto Te explicamos qué es la energía magnética, su historia, ventajas, desventajas y más características. Además, cómo funciona y…
Ver más artículos sobre Magnetismo
Narcoterrorismo
China creó una nueva cepa mutante de Covid-19 y temen que se convierta en una nueva pandemia
Fuente: El Cronista Un laboratorio chino ha creado una cepa mutante de coronavirus que ataca al cerebro de ratones. Según han indicado, esta tiene una tasa de mortalidad del 100%….
La historia del narcoterrorismo, desde las guerras del opio a los grupos yihadistas
Fuente: Lisa News El narcoterrorismo representa uno de los principales desafíos para la seguridad global y, desde el siglo XIX, impacta de diferentes formas y proporciones en todos los países…
El fentanilo como arma geopolítica: «Es la tercera guerra del opio»
Fuente: El Confidencial El Gobierno de Estados Unidos acusa a China de facilitar la llegada de fentanilo a sus fronteras, droga que causa la muerte diaria de unos 200 estadounidenses…
Ver más artículos sobre Narcoterrorismo
Argenchina
En diciembre comenzará la producción de baterías de litio en el país
Fuente: Telam En el marco de la visita del presidente Alberto Fernández a las instalaciones de Y-TEC, en el partido bonaerense de Berisso, Roberto Salvarezza aseguró que el proyecto desplegado desde YPF apunta a un desarrollo “desde el salar hasta las baterías”. El presidente de Y-TEC (YPF-Tecnología), Roberto Salvarezza, afirmó este martes que en diciembre próximo se pondrá en marcha la producción…
Metahumano
Inteligencias artificiales que conversan con humanos empezaron a mostrar síntomas de ‘depresión’
Fuente: RPP Los chatbots de inteligencia artificial están asimilando la tristeza y el nihilismo de las personas con las que conversa. El estudio…
Los zombies digitales
Fuente: CEAC Cabe recordar que esto es un blog de informática, no de cinéfilos, así que no vamos a hablar…
Lo SOCIAL
7 LECCIONES ESTOICAS VALIOSAS para CONTROLAR tus EMOCIONES según Marco Aurelio
Fuente: YouTube Embárcate en un viaje transformador hacia el dominio emocional con las 7 lecciones estoicas más valiosas, guiadas por…
La mina de litio que abastece a Tesla, BMW y General Motors secó una vega en Catamarca
Fuente: El Diario AR La utilización de agua dulce para la extracción de mineral, clave para la transición energética, provocó…
Chicos israelíes y palestinos hallaban paz en una piscina. Hasta el 7 de octubre
Fuente: The New York Times Los adolescentes del club de natación de Gran Jerusalén no se centraban en sus diferencias….
Más Noticias SOBRE
Coronavirus
Humanidad
Cerebro
Deshumanización
The Ocean CleanUp logra sacar 55 toneladas de plásticos del océano
Fuente: National Geographic En tan solo seis semanas, el proyecto ha logrado extraer una gran cantidad de desechos de la Gran Mancha de Basura del Pacífico, ubicada entre Hawái y California. Ver video: https://www.nationalgeographic.com.es/medio-ambiente/lucha-contra-el-plastico-logra-sacar-toneladas-oceano-pacifico_20656 El proyecto The Ocean Cleanup es una organización sin ánimo de lucro originaria de Países Bajos que se ha propuesto el ambicioso objetivo de limpiar de plástico los océanos…
La importancia del Olfato
Pérdida De Olfato
Fuente: YouTube En este episodio Frank explica por qué algunas personas presentan un agudo sentido del olfato mientras que otras…
¿Los mosquitos son “máquinas perfectas” de olfatear humanos?
Fuente: Infobae A diferencia de la mayoría de los animales, estos insectos pueden captar los aromas a través de vías…
El olfato de los mosquitos es (todavía) mejor de lo que pensábamos. Malas noticias para tu cuerpo
Fuente: Xataka El Aedes aegypti, el mosquito al que se conoce como del dengue o de la fiebre amarilla, es uno…
Los mosquitos tienen un olfato infalible para encontrar a quién picar
Fuente: El País Investigadoras de EE UU descubren que las hembras del ‘Aedes aegypti’ tienen varios receptores en sus neuronas…